一种分离三元锂离子电池正极浸出液中锰的方法
阅读说明:本技术 一种分离三元锂离子电池正极浸出液中锰的方法 (Method for separating manganese in ternary lithium ion battery anode leachate ) 是由 吴浩 郑江峰 高琦 黄仁忠 王苗 张颖 于 2021-07-05 设计创作,主要内容包括:本发明提供了一种分离三元锂离子电池正极浸出液中锰的方法,包括以下步骤:在三元锂离子电池正极材料的浸出液中加入复合氧化剂,使Mn~(2+)发生氧化反应,并以MnO-(2)的形式沉淀,去除所述浸出液中的锰元素;其中,所述复合氧化剂由高锰酸盐和过硫酸盐组成,所述高锰酸盐与所述过硫酸盐的摩尔比为8.5~9.5:1。该方法缩短了电池正极材料的回收流程,并且产物收率较高,锰的去除率高达98.733%,而钴、镍的损失率分别低至2.44%和0.48%。分离得到的MnO-(2)或者MnSO-(4)杂质含量低,所需设备要求简单,实验条件温和,可采用常温反应,具有良好的环保和经济效益。(The invention provides a method for separating manganese in ternary lithium ion battery anode leachate, which comprises the following steps: adding composite oxidant into the leaching solution of the ternary lithium ion battery anode material to ensure that Mn is added 2+ Oxidation reaction takes place and with MnO 2 Precipitating in a form of (1), and removing manganese element in the leachate; the composite oxidant consists of permanganate and persulfate, and the molar ratio of the permanganate to the persulfate is 8.5-9.5: 1. the method shortens the recovery process of the battery anode material, and has the advantages of high product yield and high manganese removal rate98.733%, while the loss rates of cobalt and nickel are as low as 2.44% and 0.48%, respectively. MnO obtained by separation 2 Or MnSO 4 The method has the advantages of low impurity content, simple requirement on required equipment, mild experimental conditions, capability of adopting normal-temperature reaction, and good environmental protection and economic benefits.)
技术领域
本发明涉及废旧电池回收技术领域,具体而言,涉及一种分离三元锂离子电池正极浸出液中锰的方法。
背景技术
三元锂离子电池具有能量密度高、安全和循环性能好等特点而被广泛应用于通讯电源和动力电池,尤其是在新能源汽车领域的应用。锂离子电池一般可使用年限为三年,随着新能源行业的快速发展,废旧锂离子电池的数量急剧增加,若不进行合理有效地处理,将会对环境和水资源产生不利影响,从而影响人体健康。另一方面,废旧锂电池中富含钴镍等稀贵金属,是重要的二次资源,对其进行综合回收利用具有很高的经济价值。
湿法冶金是处理废旧锂离子电池的重要方式,在处理前一般要经过处理获得正极活性材料,进而采用硫酸浸出即可。废旧锂离子电池正极材料由于成分复杂,酸浸液除了含有Ni、Co、Mn、Li等主要元素外,还含有Al、Fe等元素,一般采用调节pH值的方法去除Al和Fe两种元素,从而使得浸出液中主要存在Ni、Co、Mn和Li。Mn的含量对Ni和Co两种贵金属的回收影响较大,在目前商业化的动力型NCM523和NCM622型中Mn的含量分别为30%和20%,对于即将退役的NCM111型其Mn含量更是达到了33.3%。为了便于回收镍和钴,在回收之前需要除去浸出液中的Mn。
常见的去除锰的方法有溶剂萃取法、硫化物沉淀和氧化沉淀法。其中,溶剂萃取法萃取剂价格昂贵,过程损耗且工序复杂。硫化物沉淀法将溶液中的Ni和Co以硫化物沉淀而与Mn分离,但后续还需再处理钴镍硫化渣,浸出过程复杂、流程长。
例如,专利文件CN109244498A公开了一种废旧锂离子电池的回收再利用的方法,将废旧锂电池拆解得到活性正极片,用去离子水和乙醇清洗干燥后,加到邻苯基苯酚溶液中,再加入一定量的过硫酸氢钾复合盐,将正极材料用作催化剂。但过程复杂,生成的废水需要高级氧化技术,成本较高。专利CN107196007A提供了一种锂电池回收再利用的方法,废旧锂电池经过放电工序后,破碎研细,经过N-甲基吡咯烷酮清洗实现电池材料的溶解。但此方法引入较多的有机溶剂,增加了回收过程的资金投入,且有毒害的有机溶剂难回收,易造成大气污染和水体污染。
目前,现行的废旧锂离子电池综合回收技术主要采用还原酸浸技术,通过控制反应体系的pH值去除Al和Fe,进而获得富含Ni、Co、Mn和Li的溶液。其技术研究主要集中在正极材料分离和还原技术,混合溶液的分离研究较少,一般主要通过后续对混合溶液的萃取进行分离,但萃取过程需要配置相对应的萃取有机相及其它相应的条件,在进行除杂净化时也会损失掉一些钴镍,硫化物沉淀会生成一些难溶的硫化镍钴渣,需要再次进行湿法冶金工艺进行综合提取,整套工艺流程长、成本较高、占用空间大。
有鉴于此,特提出本发明。
发明内容
本发明的第一目的在于提供一种分离三元锂离子电池正极浸出液中锰的方法,以完全或部分解决上述问题,所述的分离三元锂离子电池正极浸出液中锰的方法,采用特定比例的高锰酸盐和过硫酸盐组成的复合氧化剂,将Mn2+氧化为Mn4+,使得Mn以MnO2的形式沉淀出来,从而实现Mn与Co、Ni的分离,并且不会引入过量的高锰酸盐,引起返锰现象,可在常温范围内进行反应。该方法还能在分离锰的同时,尽量少的损失溶液中的Co和Ni。
本发明的第二目的在于提供一种回收三元锂离子电池正极中Ni和Co的方法,该方法先采用所述的分离三元锂离子电池正极浸出液中锰的方法分离浸出液中的锰,再进行Ni和Co元素的分离,可以有效避免Mn离子对于Ni和Co元素的分离的分离,同时在分离Mn的同时尽量保留浸出液中的Ni和Co,实现废旧锂离子电池正极材料的高效利用。
为了实现本发明的上述目的,特采用以下技术方案:
本发明所提供的一种分离三元锂离子电池正极浸出液中锰的方法,包括以下步骤:
在三元锂离子电池正极材料的浸出液中加入复合氧化剂,使Mn2+发生氧化反应,并以MnO2的形式沉淀,去除所述浸出液中的锰元素;
其中,所述复合氧化剂由高锰酸盐和过硫酸盐组成,所述高锰酸盐与所述过硫酸盐的摩尔比为8.5~9.5:1。
根据发明,高锰酸盐中的高锰酸根离子和过硫酸盐中的过硫酸根均具有氧化性。通过添加高锰酸盐和过硫酸盐的复合添加剂,将Mn2+氧化为Mn4+,使得Mn以MnO2的形式沉淀出来。高锰酸盐和过硫酸盐均具有一定的氧化性,但高锰酸盐氧化生成的二氧化锰比表面积大且表面羟基较丰富,对水中阳离子具有一定的吸附性,使用时要低于理论用量,就能具有较好的锰分离效果,当高锰酸盐用量较多时高锰酸盐含有锰会引入锰离子导致“返锰”。另一方面,高锰酸盐相对容易挥发,尤其是在温度较高时,随着高锰酸盐的分解加快,会使得溶液中的氧化剂含量减少,从而导致氧化性部分失活。为了保证氧化剂活性,就需要在低温条件下进行,但增加了成本。过硫酸盐是一种较稳定的氧化剂,将其与高锰酸盐混合的复合氧化剂,可以避免单独使用高锰酸盐而导致的氧化剂分解的问题,该复合氧化剂可在常温下进行反应,使得废旧三元锂离子电池正极材料浸出液中锰的分离,并且减少Ni和Co的损失。
在本发明一些优选的实施方式中,所述复合氧化剂的添加量为所述浸出液中沉淀Mn2+理论所需的高锰酸盐的摩尔量的0.85~1.15倍,包括但不限于0.85倍、0.9倍、0.95倍、1倍、1.05倍、1.1倍、1.15倍中的任意一者的点值或任意两者之间的范围值,优选为0.95~1.05倍。
根据发明,以高锰酸钾和过硫酸钠为例,可知Mn2+的氧化过程包括以下反应:
2KMnO4+3MnSO4+2H2O=K2SO4+5MnO2↓+2H2SO4;
Na2S2O8+MnSO4+2H2O=MnO2↓+Na2SO4+2H2SO4。
通过检测浸出液中Mn2+的初始含量,上述反应可以得到高锰酸盐的理论用量(摩尔量),从而确定复合氧化剂中高锰酸盐的理论加入量,进而确定两种氧化剂的加入量。
在本发明一些优选的实施方式中,所述氧化反应的过程中,在pH在5-5.5范围内对锰的去除率影响不大,当pH大于5.5时,浸出液中的钴和镍开始沉淀,所以应控制pH上限为5.5,优选溶液体系的pH=5~5.5,包括但不限于5、5.1、5.2、5.3、5.4、5.5中的任意一者的点值或任意两者之间的范围值。
在本发明一些优选的实施方式中,所述氧化反应的过程中,该氧化过程可以在室温环境下进行,优选的溶液体系的温度为20~40℃,包括但不限于20℃、25℃、30℃、35℃、40℃中的任意一者的点值或任意两者之间的范围值。
在本发明一些优选的实施方式中,所述氧化反应的时间为10~30min,包括但不限于10min、15min、20min、25min、30min中的任意一者的点值或任意两者之间的范围值,所述氧化反应过程耗时短、分离效率高。
在本发明一些优选的实施方式中,三元锂离子电池正极材料的浸出液的制备方法包括:
将三元锂离子电池的正极材经过放电和破碎处理后,再采用酸液浸出材料中的金属元素,得到混合溶液;去除所述混合溶液中的Al元素和Fe元素,得到所述浸出液。
优选地,通过调节pH值的方式去除所述混合溶液中的Al元素和Fe元素,对浸出液进行初步纯化。具体地,金属阳离子具有对应的弱碱的饱和pH值(即SpH),高于这个pH值时,也就是低于分析浓度,即可以将这种金属阳离子从溶液中去除。氢氧化铁的SpH为3.2,氢氧化铝的SpH为4.6,所以通过逐步控制pH可以实现对Al元素和Fe元素的去除。
在本发明一些优选的实施方式中,所述酸液包括硫酸、盐酸和硝酸中的至少一种。
在本发明一些优选的实施方式中,所述酸液的质量浓度为45%-75%。
在本发明一些优选的实施方式中,所述高锰酸盐包括高锰酸钠、高锰酸钾和高锰酸钙中的一种或几种的组合;优选为高锰酸钾。
在本发明一些优选的实施方式中,所述过硫酸盐包括过硫酸钾、过硫酸铵和过硫酸钠中的一种或者几种的组合;优选为过硫酸钠。
在本发明一些优选的实施方式中,所述三元锂离子电池正极的分子式为LiNixCoyMn1-x-yO2,其中,0<x<1,0<y<1,1-x-y>0。
一种回收三元锂离子电池正极中Ni和Co的方法,包括所述的分离三元锂离子电池正极浸出液中锰的方法。
与现有技术相比,本发明的有益效果为:
(1)本发明所提供的分离三元锂离子电池正极浸出液中锰的方法,采用特定比例的高锰酸盐和过硫酸盐组成的复合氧化剂,将Mn2+氧化为Mn4+,使得Mn以MnO2的形式沉淀出来,从而实现Mn与Co、Ni的分离,并且不会引入过量的高锰酸盐,引发起返锰现象,可在常温范围内进行反应。该方法还能在分离锰的同时,尽量少的损失溶液中的Co和Ni。
(2)本发明所提供的分离三元锂离子电池正极浸出液中锰的方法,锰的去除率在96%以上,镍的损失率变化差异小,维持在0.5%左右,钴的损失率存在微小差异。
(3)本发明所提供的分离三元锂离子电池正极浸出液中锰的方法,减少了其他杂质元素的引入,缩短了回收流程、产物收率较高,带入的钾离子和钠离子在进行正极材料再生制备前驱体过程中可以通过洗涤工序去除,不影响后期使用。
(4)本发明所提供的分离三元锂离子电池正极浸出液中锰的方法,生成的MnO2或者MnSO4杂质含量低,所需设备要求简单,实验条件温和,可采用常温反应,具有良好的环保和经济效益。
(5)本发明所提供的分离三元锂离子电池正极浸出液中锰的方法,在回收三元锂离子电池正极中Ni和Co中的应用。
附图说明
为了更清楚地说明本发明
具体实施方式
或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
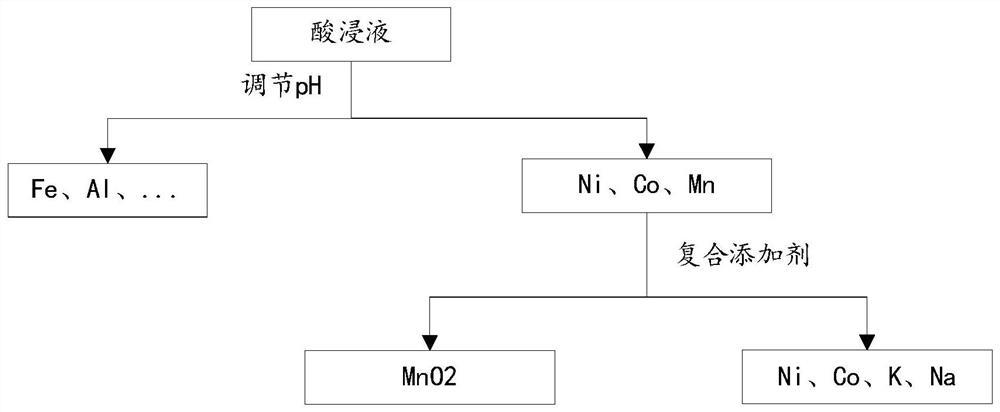
图1为本发明实施例提供的回收三元锂离子电池正极中金属离子的流程示意图。
具体实施方式
下面将结合附图和具体实施方式对本发明的技术方案进行清楚、完整地描述,但是本领域技术人员将会理解,下列所描述的实施例是本发明一部分实施例,而不是全部的实施例,仅用于说明本发明,而不应视为限制本发明的范围。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
本发明中,若无特殊说明,“三元锂离子电池”是指正极材料使用镍钴锰酸锂的锂电池。
在下述实施方式中,选择某型废旧三元锂离子电池正极材料经过酸浸后经过初步纯化后的浸出液中,金属离子的含量为:Co:19.634g/L、Ni:4.038g/L、Mn:2.638g/L、Li:2.332g/L;每个实施例中使用上述浸出液50mL。通过计算,以高锰酸钾为例,高锰酸钾的理论用量为0.0016mol。
实施例1
本实施例所提供的方法,具体包括以下步骤:
在上述锂离子电池正极浸出液中加入由高锰酸钾和过硫酸钠组成的复合氧化剂,使Mn2+发生氧化反应,并以MnO2的形式沉淀,去除所述浸出液中的锰元素,分析检测上清液中残余的锰、钴、镍的含量。
其中,复合添加剂的加入量为高锰酸钾摩尔量的理论值的1.05倍,复合添加剂中高锰酸钾和过硫酸钠的摩尔比为9:1。
氧化反应过程中,溶液的pH=5,温度为30℃,反应时间为20min。
实施例2
本实施例所提供的方法,具体包括以下步骤:
在上述锂离子电池正极浸出液中加入由高锰酸钾和过硫酸钠组成的复合氧化剂,使Mn2+发生氧化反应,并以MnO2的形式沉淀,去除所述浸出液中的锰元素,分析检测上清液中残余的锰、钴、镍的含量。
其中,复合添加剂的加入量为高锰酸钾摩尔量的理论值的1.05倍,复合添加剂中高锰酸钾和过硫酸钠的摩尔比为9:1。
氧化反应过程中,溶液的pH=5.5,温度为30℃,反应时间为20min。
实施例3
本实施例所提供的方法,具体包括以下步骤:
在上述锂离子电池正极浸出液中加入由高锰酸钾和过硫酸钠组成的复合氧化剂,使Mn2+发生氧化反应,并以MnO2的形式沉淀,去除所述浸出液中的锰元素,分析检测上清液中残余的锰、钴、镍的含量。
其中,复合添加剂的加入量为高锰酸钾摩尔量的理论值的0.85倍,复合添加剂中高锰酸钾和过硫酸钠的摩尔比为9:1。
氧化反应过程中,溶液的pH=5.3,温度为30℃,反应时间为20min。
实施例4
本实施例所提供的方法,具体包括以下步骤:
在上述锂离子电池正极浸出液中加入由高锰酸钾和过硫酸钠组成的复合氧化剂,使Mn2+发生氧化反应,并以MnO2的形式沉淀,去除所述浸出液中的锰元素,分析检测上清液中残余的锰、钴、镍的含量。
其中,复合添加剂的加入量为高锰酸钾摩尔量的理论值的0.95倍,复合添加剂中高锰酸钾和过硫酸钠的摩尔比为9:1。
氧化反应过程中,溶液的pH=5.2,温度为30℃,反应时间为20min。
实施例5
本实施例所提供的方法,具体包括以下步骤:
在上述锂离子电池正极浸出液中加入由高锰酸钾和过硫酸钠组成复合氧化剂,使Mn2+发生氧化反应,并以MnO2的形式沉淀,去除所述浸出液中的锰元素,分析检测上清液中残余的锰、钴、镍的含量。
其中,复合添加剂的加入量为高锰酸钾摩尔量的理论值的1.15倍,复合添加剂中高锰酸钾和过硫酸钠的摩尔比为9:1。
氧化反应过程中,溶液的pH=5.4,温度为30℃,反应时间为20min。
实施例6
本实施例所提供的方法,具体包括以下步骤:
在上述锂离子电池正极浸出液中加入由高锰酸钾和过硫酸钠组成的复合氧化剂,使Mn2+发生氧化反应,并以MnO2的形式沉淀,去除所述浸出液中的锰元素,分析检测上清液中残余的锰、钴、镍的含量。
其中,复合添加剂的加入量为高锰酸钾摩尔量的理论值的0.95倍,复合添加剂中高锰酸钾和过硫酸钠的摩尔比为8.5:1。
氧化反应过程中,溶液的pH=5.1,温度为30℃,反应时间为20min。
实施例7
本实施例所提供的方法,具体包括以下步骤:
在上述锂离子电池正极浸出液中加入由高锰酸钾和过硫酸钠组成的复合氧化剂,使Mn2+发生氧化反应,并以MnO2的形式沉淀,去除所述浸出液中的锰元素,分析检测上清液中残余的锰、钴、镍的含量。
其中,复合添加剂的加入量为高锰酸钾摩尔量的理论值的0.95倍,复合添加剂中高锰酸钾和过硫酸钠的摩尔比为9.5:1。
氧化反应过程中,溶液的pH=5.2,温度为30℃,反应时间为20min。
实施例8
本实施例所提供的方法,具体包括以下步骤:
在上述锂离子电池正极浸出液中加入由高锰酸钾和过硫酸钠组成的复合氧化剂,使Mn2+发生氧化反应,并以MnO2的形式沉淀,去除所述浸出液中的锰元素,分析检测上清液中残余的锰、钴、镍的含量。
其中,复合添加剂的加入量为高锰酸钾摩尔量的理论值的0.95倍,复合添加剂中高锰酸钾和过硫酸钠的摩尔比为9:1。
氧化反应过程中,溶液的pH=5.3,温度为20℃,反应时间为20min。
实施例9
本实施例所提供的方法,具体包括以下步骤:
在上述锂离子电池正极浸出液中加入由高锰酸钾和过硫酸钠组成的复合氧化剂,使Mn2+发生氧化反应,并以MnO2的形式沉淀,去除所述浸出液中的锰元素,分析检测上清液中残余的锰、钴、镍的含量。
其中,复合添加剂的加入量为高锰酸钾摩尔量的理论值的0.95倍,复合添加剂中高锰酸钾和过硫酸钠的摩尔比为9:1。
氧化反应过程中,溶液的pH=5.3,温度为40℃,反应时间为20min。
实施例10
本实施例所提供的方法,具体包括以下步骤:
在上述锂离子电池正极浸出液中加入由高锰酸钾和过硫酸钠组成的复合氧化剂,使Mn2+发生氧化反应,并以MnO2的形式沉淀,去除所述浸出液中的锰元素,分析检测上清液中残余的锰、钴、镍的含量。
其中,复合添加剂的加入量为高锰酸钾摩尔量的理论值的0.95倍,复合添加剂中高锰酸钾和过硫酸钠的摩尔比为9:1。
氧化反应过程中,溶液的pH=5.2,温度为20℃,反应时间为10min。
实施例11
本实施例所提供的方法,具体包括以下步骤:
在上述锂离子电池正极浸出液中加入由高锰酸钾和过钠组成的复合氧化剂,使Mn2+发生氧化反应,并以MnO2的形式沉淀,去除所述浸出液中的锰元素,分析检测上清液中残余的锰、钴、镍的含量。
其中,复合添加剂的加入量为高锰酸钾摩尔量的理论值的0.95倍,复合添加剂中高锰酸钾和过硫酸钠的摩尔比为9:1。
氧化反应过程中,溶液的pH=5.4,温度为20℃,反应时间为30min。
实施例12
本实施例所提供的方法,与实施例10基本相同,不同的是:复合氧化剂由高锰酸钠和过硫酸钾组成,二者的摩尔比为9:1。
对比例1
本实施例所提供的方法,与实施例10基本相同,不同的是:只采用单一氧化剂高锰酸钾。
对比例2
本实施例所提供的方法,与实施例10基本相同,不同的是:只采用单一氧化剂过硫酸钠。
试验例
采用实施例1-12和对比例1-2所提供的方法分离三元锂离子电池正极浸出液中的锰后,取上清液,分析检测上清液中残余的锰、钴和镍的含量,通过残余的元素含量来判断分离去除效果。
溶液中元素含量的检测方法采用ICP-AAS设备测得:
实施例1-12以及对比例1-2的参数对比如表1所示。
表1实施例及对比例中参数对比
检测结果如表2所示。
表2锰的去除率以及钴、镍的损失率
实验结果表明,采用本发明所提供的方法,可以有效去除浸出液中的锰离子,锰的去除率均在96%以上,镍的损失率变化差异小,维持在0.5%左右,钴的损失率存在微小差异,不到0.5%。
对比实施例1和实施例2可知,pH在5-5.5范围内对锰的去除率影响不大,当pH大于5.5时钴镍开始沉淀,所以应控制pH上限为5.5。
对比实施例3、4和5可知,随着复合添加剂比例的增加,钴的损失率逐渐增加,当添加比例较低时,由于氧化剂数量有限,导致锰的氧化不完全,所以去除率略低,当复合添加剂比例较高时,会出现“返锰”现象,这是因为高锰酸钾本身含有锰元素,超过反应所需要的氧化剂含量时会再次带入锰离子,值得注意的是,当复合添加剂的量为理论含量的0.95倍时表现出了良好的锰的去除率,这是因为高锰酸钾氧化生成的二氧化锰比表面积大且表面羟基较丰富,对水中阳离子具有一定的吸附性,一般使用时要低于理论用量,就能具有较好的锰分离效果。
对比实施例6和7可知,复合添加剂制备过程中高锰酸钾的添加比例越高,Mn的去除率越高,这是因为高锰酸钾的氧化性更强。
对比实施例4、8和9可知,随着反应温度的升高,锰的去除率有所下降,这是因为硫酸体系浸出时,随着反应温度升高,硫酸的表观电离度增加,会增加氢离子数量、降低体系pH,虽然强酸性会增加高锰酸钾的氧化性,但还原产物为Mn2+,与此同时加热会促进高锰酸钾的分解,但锰的去除率变化差异小,这是因为过硫酸钠的加入会减缓高锰酸钾的分解,保证了反应的进行。
对比例10和11可知,随着反应时间的延长,溶液中残余锰的含量反而上升,这是因为酸浸过程会加入还原剂,酸浸液中残余的少量还原剂与反应生成的二氧化锰发生了反应,使得锰“返溶”又进入了溶液。
由对比例1和2可知,当全部采用高锰酸钾和过硫酸钠时,锰的去除率较实施例10略有下降,但是钴的损失率却高于实施例10。因此,采用两种氧化剂不仅可以提高锰的回收率,同时可以减少镍和锰的损失,是一种废旧三元锂离子电池浸出液中锰的高效去除方法。
其中,实施例10为该浸出液中锰的最优去除工艺:反应过程pH在5-5.5,复合氧化剂的加入量为高锰酸钾的理论加入量的0.95倍,复合添加剂的中高锰酸钾与过硫酸钠的摩尔比为9:1,氧化反应时间为10min,反应温度为20℃时,可以获得锰的最佳浸出效果和较低的钴、镍损失率。通过分析检测上清液中残余的锰含量以及钴、镍的损失率。锰的去除率为98.733%,此时钴、镍的损失率分别为2.44%和0.48%,并且该方法反应时间短,仅需要10分钟,去除效率高。
综上,本申请所提供的分离三元锂离子电池正极浸出液中锰的方法,减少了其他杂质元素的引入,大大缩短了正极材料中各元素的回收流程,且分离得到的产物MnO2或者MnSO4杂质含量低、收率较高,带入的钾离子和钠离子在进行正极材料再生制备前驱体过程中可以通过洗涤工序去除,不影响后期使用。该方法所需的设备要求简单,实验条件温和,可采用常温反应,具有良好的环保和经济效益。
实施例13
一种回收三元锂离子电池正极中Ni和Co的方法,参考图1的流程,在初步纯化去除浸出液中的Fe和Al以后,通过实施例10的方法分离其中的Mn,最后回收溶液中的Ni和Co。
尽管已用具体实施例来说明和描述了本发明,然而应意识到,以上各实施例仅用以说明本发明的技术方案,而非对其限制;本领域的普通技术人员应当理解:在不背离本发明的精神和范围的情况下,可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围;因此,这意味着在所附权利要求中包括属于本发明范围内的所有这些替换和修改。
- 上一篇:一种医用注射器针头装配设备
- 下一篇:一种镍基高温合金屑料的处理装置及方法
